发布日期:2023-11-01 来源: 网络 阅读量( )
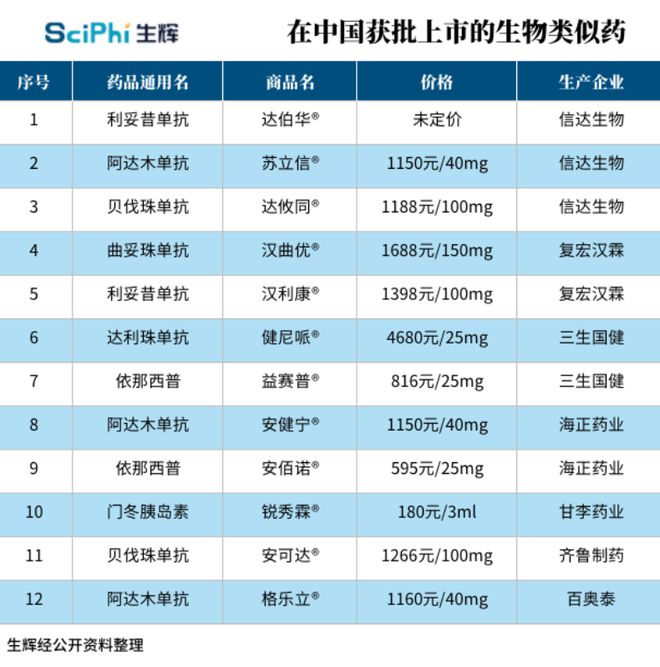
天博官方网站生物类似药带量采购将至?互换性问题尚未达成一致专家评议:难度很大需要慎重10 月 9 日,国家医疗保障局官网公布了对十三届全国三次会议第 6450 号建议的答复。其中,国家医保局称,“正在研究生物制品集中采购相关政策,生物类似药并非集中带量采购的禁区,在考虑生物类似药的相似性、企业产能和供应链的稳定性天博官方网站、具体产品的临床可替代性等因素的基础上,将适时开展集中带量采购 生物类似药(Biosimilar),也被称为生物仿制药,是与已批准的生物原研药相似的一种生物药,包括疫苗、血液及血液成分、体细胞、基因治疗、组织和重组治疗性蛋白等。 伴随着原研生物药专利陆续到期以及生物药需求的不断增长,生物类似药自问世以来便受到高度关注。据前瞻产业研究院统计,2019 年全球生物类似药市场规模约为 95 亿美元,2015 年 - 2019 年的复合年增长率约为 37.5%。 近年来,我国生物类似药的研发上市进程显著加快,经生辉的不完全统计,自 2019 年 2 月复宏汉霖的利妥昔单抗注射液(汉利康 )上市后,目前国内已有 12 款生物类似药获批上市。 从上表可以看出,阿达木单抗注射液目前国内获批上市最多的种类,有 3 家企业同台角逐;贝伐珠单抗、利妥昔单抗和曲妥珠单抗亦是研发重点。 根据米内网数据,2019 年重点省市公立医院终端使用的抗体药物用药金额超过 72 亿元,其中居前三的品种是曲妥珠单抗、贝伐珠单抗和利妥昔单抗,市场份额分别为 25.32%、20.26% 和 18.51%。 曲妥珠单抗原研药赫赛汀(Herceptin)由罗氏(Roche)研发,是一款靶向人表皮生长因子 2(HER2)的重组 DNA 衍生的人源化单克隆抗体,在 HER2 阳性乳腺癌症用药方案中占据重要地位。 2020 年 8 月 12 日,复宏汉霖的曲妥珠单抗(汉曲优 )在国内正式获批上市,全球受抗体类药物生物类似药冲击,但国内市场增长依然坚挺,呈现出逐年增长态势。 公开数据显示,截至 2020 年上半年,有 7 家本土药企的曲妥珠单抗已进入 III 期临床,分别是嘉和生物、海正药业、正大天晴、上海生物制品研究所、安科生物、华兰基因和艾迈医疗。随着国产曲妥珠单抗生物类似药的陆续上市,价格有望进一步亲民,从而满足国内患者的需求。 排名第二的贝伐珠单抗(bevacizumab,Avastin)是一种重组人源化免疫球蛋白 G1(IgG1)单克隆抗体,可以结合 VEGF-A,抑制其与 VEGF 受体 - 2(VEGFR-2)结合,继而抑制 VEGF 的生物学作用,包括影响血管的渗透性、增生以及内皮细胞迁移与存活,达到抑制肿瘤血管生成、生长以及转移的效果。 相关数据显示,2019 年重点省市公立医院终端贝伐珠单抗用药金额 14.66 亿元,同比增长 48.50%;中国公立医疗机构终端贝伐珠单抗约在 35 亿元市场规模。目前,天广实、百奥泰、恒瑞医药、正大天晴、华兰生物等企业均在进行 III 期临床试验。 利妥昔单抗(Rituxan)是罗氏旗下的骨干品种,自上市以来,全球已批准其用于治疗包括非霍奇金淋巴瘤(NHL)、慢性淋巴细胞性白血病(CLL)、类风湿性关节炎(RA)、血管炎肉芽肿(GPA)、显微镜下多血管炎(MPA)和中重度天疱疮(PV)等多个适应症,其显著的疗效和良好的安全性已得到普遍认可。 据米内网数据,2019 年重点省市公立医院终端利妥昔单抗用药金额 13.39 亿元,同比上一年增长 11.35%,中国公立医疗机构终端达到了 41.29 亿元市场规模。除复宏汉霖和信达生物已有产品上市外,正大天晴、华兰基因等企业都有布局,有望实现放量。 生物类似药一旦开始施行带量采购政策对上述企业来说是机遇还是挑战?或许我们能从化学仿制药的带量采购发展现状看出一些端倪。 带量采购始于 2018 年。2018 年 11 月 14 日,中央全面深化改革委员会第五次会议审议通过《国家组织药品集中采购试点方案》,明确了国家组织、联盟采购、平台操作的总体思路。 2018 年 11 月 15 日,经中央全面深化改革委员会同意,国家组织药品集中采购试点,试点地区范围为北京、天津、上海、重庆和沈阳、大连、厦门、广州、深圳、成都、西安 11 个城市(以下简称“4+7”),并发布文件《4+7 城市药品集中采购文件》 ,其中文件注明在化学药品的采购时,需要约定采购量。截至 2020 年 5 月,除陕西外,在国家带量采购常态化的背景下,中国已有福建、湖北、湖南、云南、山西、江西、安徽、青海等多个省级联盟甚至跨区域联盟采购相继落地,成为倒逼更多药品实现大降价的主力。 其中,2019 年 9 月的 “4+7” 带量采购扩面招投标信息公布,给医药和资本市场带来一片哗然。 从仿制药板块来看,所谓带量采购,就是国家按需拟定药物清单,各大药企以拍卖出价的形式竞标,具体的情况分为两种,企业竞标取 “最低价” 优先,如多家企业最低价相同,则按照企业的药物销售所占市场份额的高低为划分标准,选取份额较高的企业。 为了防止 “价格战” 的发生,我国利用 “扩面招投” 予以缓和。仿制药企中标后,采购量会有保障,如果三家中标,采购量会达到总需求量的 70%,继而以量换价,过往药企的营销费用、医院开发费用将急剧降低,同时,批量生产后生产成本的下降,这些都将是竞标企业降价的合理解释。 2018 年降价 73.15% 的瑞舒伐他汀,2019 年扩招后最低中标价再度下降 74.31%;2018 年降价 92.11% 的恩替卡韦分散片,2019 年最低中标价再度下降 70.58%。在 2019 年招标的 25 个品类中,共有 8 个品类在去年降价的基础上,再度降价超 50%。 上海市卫生和健康发展研究中心主任金春林曾在《21 世纪经济报道》的采访中表示,中标企业数量扩大了,原则上竞价的压力降低了。但是很多企业经过两次的实践,还是存在 “囚徒困境” 效应,如果不中标马上“死”,为了中标可能会不惜一切代价报出匪夷所思的价格,因为越不中标以后机会越少。 中信证券的研究报告也评价到,带量采购,让仿制药价格断崖式下降,然而,这种状态难以持久,利润率不能支撑,预计稳定状态下,降价较带量采购前平均约下调 50% 左右。而且成本控制和产能控制将是仿制药的核心竞争力,销售能力将不再是主要竞争要素。 “仿制药”并不鲜见,业内常用其形容化学药品。生物药的独特性在于,其一般是从动物脏器中获得的治疗药物,因此被称为 “生物制品”。疫苗,胰岛素、单抗等药物都隶属其中。“凡是来自于动物、脏器、细胞组织的药物,我们都叫做生物制品。”国家药监局评审专家孙忠实在接受生辉的采访中解释到。 孙忠实提到,“生物制品也有仿制药,但经过多年观察,业内发现生物制品的仿制药是不可能做出来的。因为它的本质是蛋白质天博官方网站,蛋白质的空间结构因人种而异,即使是同样功能的生物制品,本质上的蛋白质结构是完全不同的。”因此全球药品管理机构就你定了一个新的名词天博官方网站,不叫生物仿制药,而改为生物类似药。 “这就决定了对仿制药和生物类似药带量采购的质量管理标准是完全不同的。”目前,化学仿制药的带量采购采用”一致性评价”体系来筛选标的药物和企业。孙忠实反复强调:“生物类似物从生产到获批,需要更为严格的质量把控,比化学仿制药的标准高出许多。” 对于化学药品而言,监管部门只需要检测分子结构和质量来确定药物的质量,生物类似药则有一条独特的衡量指标——免疫原性。 “生物药作为‘抗原’进入后很容易引起免疫反应,所以除了其他评定条件跟化学仿制药要求一致外,需要特别关注生物类似药作用于后会不会引发异体排斥反应。”孙忠实表示。 同时,孙忠实也提到,因为免疫原性把控不及时,人类已经受到过很多历史教训。“有一段时间美国 FDA 就曾停止了生物类似药的批准,直到把控的条件日趋成熟才将其开放。”事实上,对于生物类似药的互换性问题,目前全球也尚未达成一致。 孙忠实认为,对于老百姓而言,一定要知道什么叫做生物类似药,确保它的安全性、有效性;对于监管机构而言,一定要建立比化学药仿制药更加高标准、严要求的质量评定标准;对于生产生物类似药的企业而言,一定要遵纪守法,按照国家的标准,坚决落实,不能含糊。 面对生物类似药如此严格质量把控标准,化学仿制药的 “一致性评价” 无法完全平移到 “生物类似药” 的评判过程中,这会给未来生物类似药带量采购的真正落地带来哪些影响?药智网联合创始人李天泉告诉生辉,他对这一标准的实行持不完全乐观态度。 李天泉告诉生辉,生物类似药的研发投入比化学药仿制大得多,药厂做一个化学仿制药差不多需要投入 1000 万元的研发经费,在大量生产的情况下,实际投入的研发成本很低。但生物类似药物不同,其研发难度、周期性、风险性等问题均是化药仿制药无法对比的。 “有些生物类似药的生产,我们国家也才在刚刚起步,所以我认为还是需要慎重。前期应该鼓励药企先把真正的生物类似药做出来,可能不需要过早地推出集中采购。现在针对生物类似药,我认为应该是以鼓励为主,如果过早地集采,可能会打消企业对药物研发的积极性。”李天泉表示。 在上述背景下,生物类似药实行 “带量采购” 这一政策真正从 “意向” 变为 “现实” 还需要多久? 孙忠实和李天泉的观点十分一致:最快也需要等到明年这个时候,这是最乐观的时间估计。“从‘意向’到‘落地施行’,我们需要做的前期准备工作还有太多太多。”